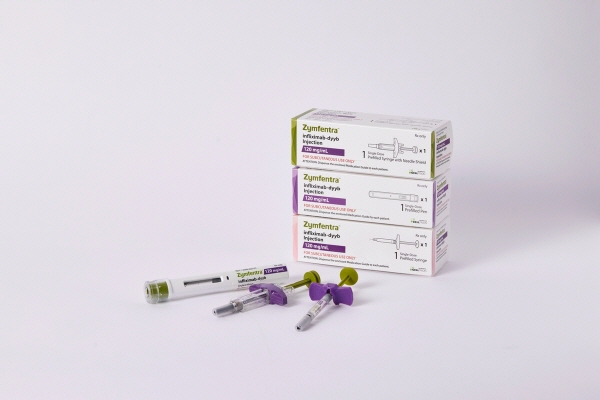
셀트리온은 15일(현지시간) 인플릭시맙 피하주사(SC) 제형인 ‘짐펜트라’(램시마SC 미국 제품명)를 미국 전역에 출시하며 시장 공략에 본격 돌입했다고 18일 밝혔다.
짐펜트라는 셀트리온이 지난해 10월 미국 식품의약국(FDA)으로부터 신약 허가를 받은 제품이다. 중등도 내지 중증의 성인 활성 궤양성 대장염(Ulcerative Colitis)과 크론병(Crohn’s Disease) 환자 대상으로 허가를 받았다. 권장 용량은 2주 간격으로 회당 120mg이다.
이 신약은 기존 셀트리온의 정맥주사 제형 자가면역질환 치료제 바이오시밀러(바이오의약품 복제약)인 ‘램시마’(성분명 인플릭시맙)를 자가 투여가 가능한 피하주사 제형으로 변경해 개발한 제품이다. 지난해 10월 미국 식품의약청(FDA)으로부터 신약으로 허가받았다.
짐펜트라의 도매가격(WAC‧Wholesale Acquisition Cost)은 6181.08달러(2회 투여분‧4주 기준)로 책정됐다. 한화 기준으로는 약 823만원에 달한다. 셀트리온은 짐펜트라의 신약 지위와 염증성 장질환(IBD) 경쟁 의약품 가격, 미국 제약바이오 시장 특성 등을 종합적으로 고려해 효과적인 판매 전략을 운영할 수 있는 최적의 가격 정책을 수립했다고 설명했다.
짐펜트라는 현재 출원된 SC제형과 투여법에 대한 특허가 등록되면 최대 2040년까지 특허 보호를 받을 수 있다. 세계 최대 제약 시장인 미국에서 안정적인 중장기 수익성 확보가 가능할 것으로 전망된다.
의약품 시장조사기관인 아이큐비아(IQVIA)에 따르면 인플릭시맙을 포함한 미국 TNF-α 억제제 시장은 2022년 기준 약 62조570억원 규모다. 이 가운데 짐펜트라가 주력하는 IBD 시장 규모는 12조8000억원에 이른다. 셀트리온은 출시 2년 차인 2025년을 목표로 타깃 환자 처방률을 10% 이상 달성해 짐펜트라를 연 매출 1조 원 이상의 글로벌 블록버스터 제품으로 등극시킨다는 계획이다.
짐펜트라는 미국 현지 법인을 통해 셀트리온이 직접 판매할 예정이다. 시장 공략을 위해 적극적인 마케팅 활동을 펼쳐가고 있다. 이미 복수의 중소형 처방약급여관리업체(PBM)에서 짐펜트라의 경쟁력을 인정해 별도 협상 없이 자체적으로 자사 처방집(formulary)에 제품을 등재하는 등 출시 초반부터 처방 확대를 위한 기반이 마련되고 있다. 셀트리온은 대형 PBM과도 2분기 내 선호의약품 등재를 목표로 협상을 이어가고 있다.
셀트리온은 올해 미국에서 개최되는 학회들에 참가해 현지 의료진들에게 직접 짐펜트라의 제품 경쟁력을 알릴 예정이다. 환자들 대상으로도 보험 지원이 충분하지 않은 이들에게 제품 할인 및 공급 등을 지원하는 지원 프로그램도 운영할 방침이다.
파이낸셜투데이 신용수 기자